Entalpia
Entalpia właściwa h [kJ/kg] oznacza całkowitą ilość ciepła zawartego w parze.
Entalpia dzieli się na ciepło jawne, które wywołuje zmiany temperatury, oraz ciepło utajone („ukryte”), gdy przy stałej temperaturze udział pary zmienia się od 0 do 100 %.
Dostarczanie energii cieplnej powoduje ogrzewanie się wody aż do osiągnięcia linii wrzenia. Gdy linia wrzenia zostaje osiągnięta, przy dalszym dostarczaniu energii rośnie zawartość pęcherzyków pary w objętości wody, dopóki cała woda nie zmieni się w parę.
Entalpia właściwa parowania r wody wyrażona w [kJ/kg] oznacza taką ilość energii cieplnej, która musi zostać doprowadzona do 1 kg wody, aby woda przeszła ze stanu ciekłego w stan gazowy. W kotle doprowadzenie ciepła odbywa się przy stałym ciśnieniu, w związku z tym nie występuje także wzrost temperatury, stąd ta energia cieplna jest nazywana ciepłem utajonym.
Odwrotny proces zachodzi przy oddawaniu ciepła. Najpierw para skrapla się, oddając ciepło utajone ogrzewanemu czynnikowi, aż całkowicie zmieni się w wodę (faza ciekła). Dopiero wtedy następuje oziębienie kondensatu. To oziębienie kondensatu jest też często nazywane przechłodzeniem poniżej temperatury linii wrzenia, odpowiadającej danemu ciśnieniu pary.

|
Ciepło jawne Ciepło utajone |
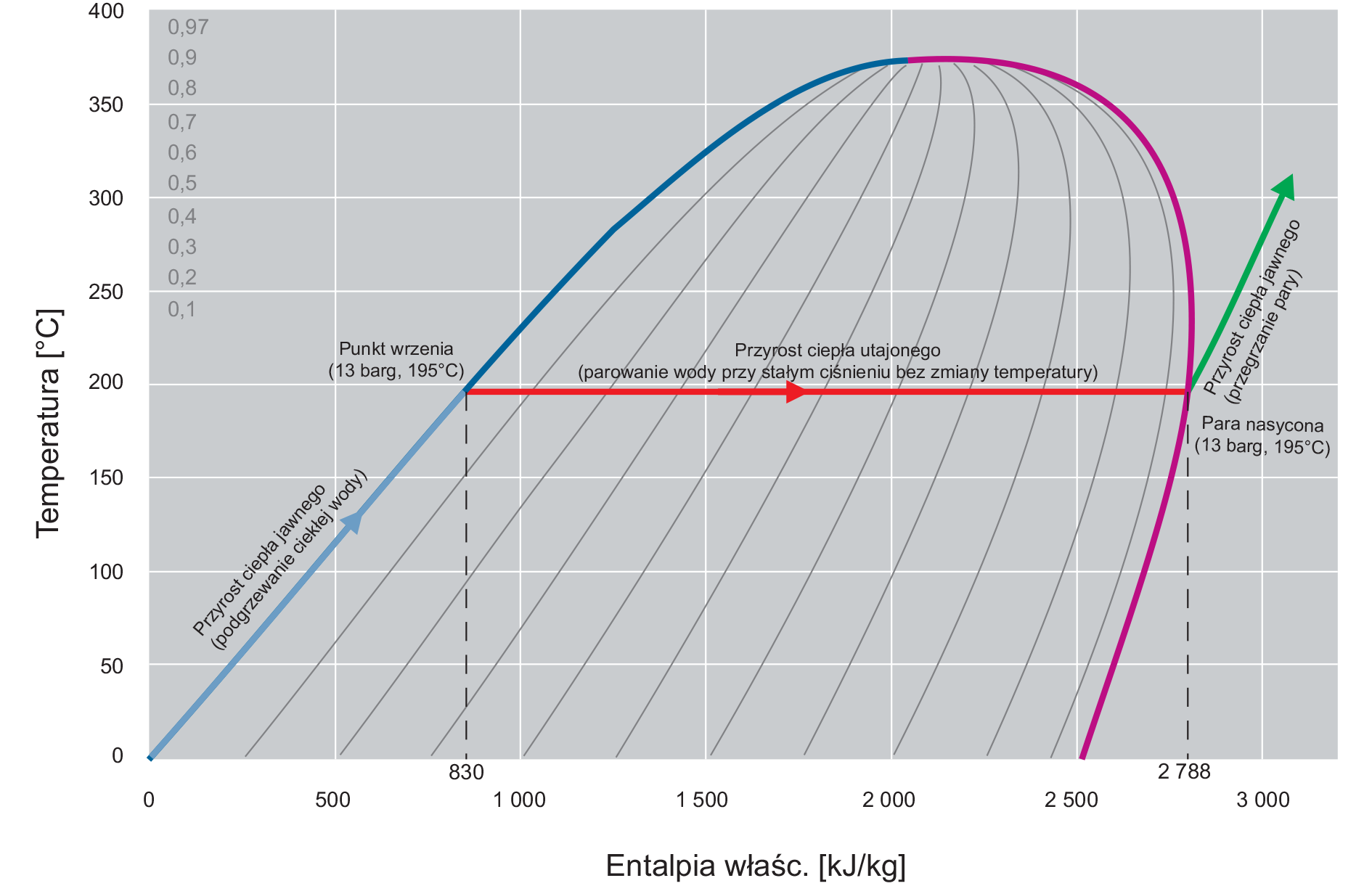
Koncepcja ciepła jawnego i utajonego na wykresie zależności entalpii od temperatury (wykres T-h)
|
|
Ciecz nasycona |
|
Woda pod ciśnieniem |
|
Para przegrzana |
||
|
|
Para nasycona |
|
Para mokra |




